Хиноны
Строение хинонов
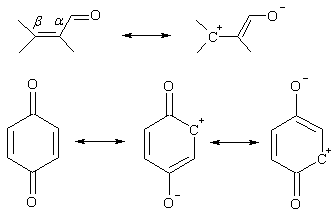
Подобно нециклическим α,β-непредельным карбонильным соединениям в молекулах хинонов имеет место разделение зарядов между концевыми атомами сопряженной системы. При этом на карбонильных атомах углерода хиноидной структуры локализован частичный положительный заряд, а атомы кислорода несут частичный отрицательный заряд. Это явление легко представить с помощью резонансных структур

π-Дефицитность
Примером проявления этого свойства хинонов является образование молекулярных комплексов с электроноизбыточными соединениями. Так, хингидрон – молекулярный комплекс пара-бензохинона (акцептора) и гидрохинона (донора) – темно-зеленые кристаллы, образующиеся как при взаимодействии пара-бензохинона и гидрохинона, так и, в качестве промежуточного продукта, при окислении гидрохинона или восстановлении пара-бензохинона.

Как и для α,β-непредельных кетонов для хинонов характерны реакции 1,4-присоединения. Хиноны присоединяют галогенводородные и карбоновые кислоты, спирты, алифатические и ароматические амины. Например, пара-бензохинон присоединяет хлороводород, превращаясь в хлоргидрохинон.


Механизм этого превращения включает стадии протонирования карбонильного атома кислорода, атаку хлорид-аниона по электронодефицитному атому углерода и таутомеризацию образовавшегося хлоркетона.


Подобно кетонам хиноны реагируют с гидроксиламином, образуя моно- или диоксимы.

Хиноны в качестве диенофилов вступают в реакции диенового синтеза. Например, при нагревании эквимольных количеств пара-бензохинона и 1,3-бутадиена образуется аддукт, который таутомеризуется в производное 1,4-дигидронафталина. При использовании избытка 1,3-бутадиена реакция протекает по обеим двойным С=С-связям пара-бензохинона.

Хиноны легко восстанавливаются до двухатомных фенолов при действии различных восстановителей – дитионита натрия, алюмогидрида лития, борогидрида натрия, цинка в уксусной кислоте, олова в соляной кислоте и других. Например, при восстановлении пара-бензохинона образуется гидрохинон.

На этой особенности хинонов основано их использование в реакциях органического синтеза в качестве окислителей. Так, хиноны с высоким окислительно-восстановительным потенциалом – 2,3,5,6-тетрахлор-1,4-бензохинон (хлоранил), 2,3-дихлор-5,6-дициано-1,4-бензохинон (ДДХ) – применяются в реакциях получения ароматических соединений путем дегидрирования неароматических или частично гидрированных ароматических предшественников. 1,2,3,4-Тетрагидронафталин (тетралин) при нагревании с хлоранилом превращается в нафталин, а неароматический 1,3,5-циклогептатриен (тропилиден) – дегидрируется с образованием соли тропилия.
