Аминокислоты
Белки
Белки и полипептиды – это природные полимеры, состоящие из остатков аминокислот, связанных амидной (пептидной) связью. Условно считают, что пептиды имеют в своем составе до 100 мономерных единиц аминокислот, а белки – свыше 100. В свою очередь пептиды делятся на олигопептиды – до 10 структурных единиц и полипептиды – от 10 до 100 структурных единиц. Другое различие белков и пептидов – пространственное. Для каждого белка гибкая полипептидная цепь имеет характерную трехмерную пространственную структуру, причем функции белков в живых организмах в основном обусловлены этим пространственным строением. Практически все белки построены из остатков 20 α-аминокислот (всего в природе встречается около 70 аминокислот), соединенных в одну или несколько неразветвленных полиамидных цепей. Анализ и синтез сложных белковых молекул – одна из важнейших задач органической химии. В этой области органическая химия тесно связана с биологией, биохимией, медициной и фармакологией. Белки – это основа органической жизни, и, следовательно, большое количество лекарственных препаратов имеют белковую структуру. К ним, в частности, относятся, антибиотики грамицидин и циклоспорин, гормоны окситоцин и инсулин, противовирусные интерфероны, иммуностимулирующие иммуноглобулины.
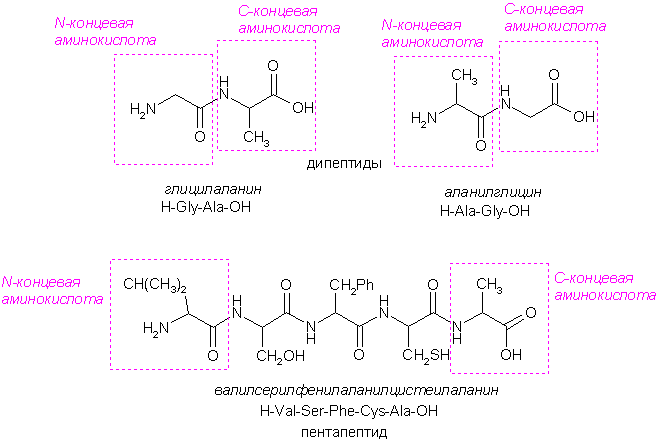
Названия пептидов строятся перечислением остатков аминокислот начиная с N-концевой аминокислоты, в которых окончание –ин заменено на –ил. Название последней (С-концевой) аминокислоты не изменяется. Гораздо чаще формулы пептидов записывают в виде сокращенных названий аминокислот.

Формально образование пептидной цепи можно представить следующей схемой:
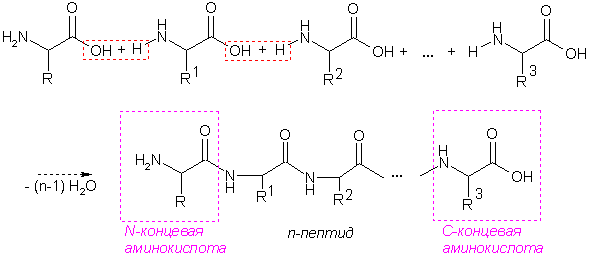
Для получения пептида недостаточно иметь необходимые аминокислоты, ведь из двух аминокислот можно получить два различных дипептида (с учетом возможности самоконденсации – четыре дипептида), из трех – шесть различных трипептидов, и т. д. Так как необходимо «собрать» молекулу белка, строго соблюдая последовательность аминокислотных остатков, в синтезе пептидов используют приемы защиты аминогруппы и активирования карбоксильной группы.
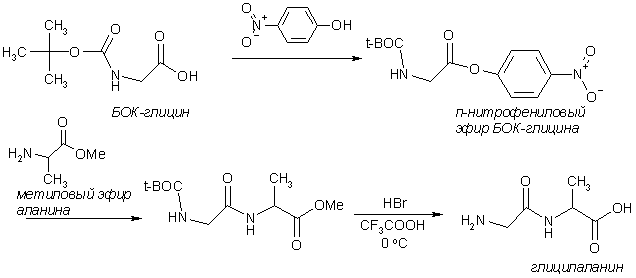
Например, чтобы синтезировать дипептид глицилаланин осуществляют следующие стадии: 1) защита аминогруппы глицина введением БОК-группы (См. Ацилирование аминокислот); 2) активирование карбоксильной группы БОК-глицина, например, переводом его в п-нитрофениловый эфир; 3) блокирование карбоксильной группы аланина переводом в метиловый эфир (См. Этерификация аминокислот); 4) синтез защищенного по обоим концам дипептида; 5) снятие защит.
Весьма перспективен твердофазный синтез пептидов (метод Меррифильда) в котором наращивание пептидной цепи происходит на поверхности полимера. В качестве подложки (носителя) обычно используют хлорметилированный (-СH2Cl) или гидроксиметилированный (-CH2OH) полистирол, в котором содержание групп СH2Cl или CH2OH не превышает 1-2 %. Использование твердофазного синтеза позволяет исключить стадию активации карбоксильной группы. Например, твердофазный синтез глицилвалилфенилаланина включает следующие этапы: 1) получение БОК-защищенного фенилаланина; 2) присоединение БОК-фенилаланина к носителю; 3) удаление защитной группы; 4) добавление БОК-валина; 5) снятие защиты; 6) добавление БОК-глицина; 7) удаление защиты и снятие трипептида с полимера.

Твердофазный синтез имеет ряд преимуществ. Во-первых, поскольку на каждой стадии продукт реакции является полимером, то, обладая пониженной растворимостью, легко очищается (отмывается) от реагирующих веществ. Во-вторых, твердофазный синтез успешно поддается автоматизации. Например, с помощью автоматизированного пептидного синтеза налажен промышленный выпуск синтетического аналога гормона инсулина, состоящего из 51 аминокислотного остатка.