
Гетероциклические соединения
Химические свойства. Пиррол
Основность
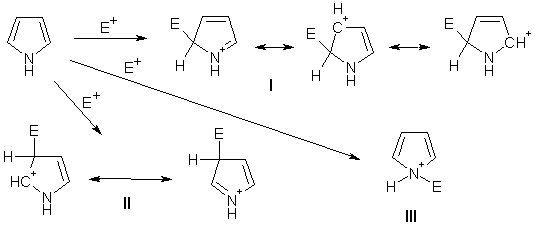
Неподеленная пара электронов пиррольного азота в значительной степени вовлечена в циклическое π-сопряжение, она малодоступна, и поэтому пиррол проявляет весьма низкую основность (pKa сопряженной кислоты = – 3,8). Расчеты показывают, что среди возможных катионов пиррола термодинамически наиболее выгоден резонансно-стабилизированный катион I – результат протонирования атома углерода в α-положениях. N-катион III наименее стабилен, т.к. во-первых, заряд в нем сосредоточен на одном атоме, и, во-вторых, нарушена ароматическая система сопряжения: это – фактически диен. Катион II занимает промежуточное положение.

Кристаллические соли, соответствующие катионам типа I, могут быть выделены при пропускании сухого HCl через растворы полиалкилпирролов в инертных растворителях. Нужно отметить, что несмотря на энергетическую невыгодность катиона III он образуется быстрее всех прочих. Доказательством этого является более легкий дейтерообмен протона при пиррольном атоме азота по сравнению с углеродом в кислой среде. Такое явление называется кинетической основностью. Кинетическая основность азота всегда выше, чем углерода.
С-катион II отвечает за процесс полимеризации пиррола в кислой среде, когда образуется полимер переменного строения «пиррол-красный». Механизм первых стадий этой реакции подтвержден строением выделенного тримера.

Склонность пирролов к полимеризации под действием кислот накладывает серьезные ограничения на участие пирролов в реакциях с электрофилами, т.к. многие превращения такого типа требуют наличие кислой среды.
Реакции по атому азота
Кислотность пиррола (рКа 17,0) близка к кислотности этанола (рКа 15,9), и сильные основания способны превратить его в пиррил-анион, который представляет собой высоко π-избыточный гетероаналог циклопентадиенила. Получаемые действием амидов металлов или щелочных металлов натриевые и калиевые соли пиррола легко взаимодействуют с электрофилами – алкилируются и ацилируются по атому азота, – тогда как смешанные N-пиррилмагнийгалогениды (связь N–Mg менее ионная, чем N-Na) реагируют преимущественно по α-положению ядра.

Кинетический продукт ацилирования – N-ацилпиррол – в отсутствии катализатора при нагревании перегруппировывается в более термодинамически устойчивый продукт – 2-ацетилпиррол.

Реакции по атомам углерода
В нейтральной и кислой среде пирролы почти никогда не реагируют с электрофилами по атому азота. Электрофильная атака направляется, главным образом, в α-положения ядра. Это объясняется тем, что образующиеся при этом σ-комплексы типа I, как и в случае протонирования, наиболее стабильны среди всех возможных.
Нитрование
Нитрующая смесь вызывают быстрое разложение пиррола, поэтому для нитрования используют специальные реагенты: ацетилнитрат, приготавливаемый заранее из 70%-ной HNO3 и уксусного ангидрида, либо кристаллический тетрафторборат нитрония в неводных растворителях. Во втором случае (более мягкий реагент) выходы выше. Соотношение α- и β-изомеров составляет примерно 4 : 1.

Сульфирование
Сульфирование пиррола по причине его ацидофобности олеумом невозможно; однако, пиррол-2-сульфокислота образуется с хорошим выходом при использовании комплекса SO3 с пиридином, который называется пиридинсульфотриоксидом.

Ацилирование
Ацилирование пирролов по атомам углерода, в отличие от бензола, не требует применения катализаторов, используемых обычно в реакции Фриделя-Крафтса. Пиррол настолько активен, что реагирует при нагревании с уксусным ангидридом, при этом легко могут быть получены как 2-ацил-, так и 2,5-диацилпирролы.

Алкилирование пиррола по Фриделю-Крафтсу редко применяется в синтетических целях, т.к. при этом быстро образуются полиалкилпроизводные.
Галогенирование
Взаимодействие пирролов с молекулярными галогенами приводит, как правило, к замещению всех свободных атомов водорода; в то же время сульфурилхлорид при охлаждении монохлорирует пиррол в α-положение.

Моногалогенпирролы, в отличие от полизамещенных соединений, неустойчивы.
Галогенирование пирролов протекает столь активно, что зачастую сопровождается отщеплением заместителей, например, карбоксильной группы, в свою очередь атом галогена, чаще всего иода, легко удаляется при гидрировании. Это позволяет получить незамещенное положение в ядре в том случае, когда более доступным в качестве исходного соединения оказывается замещенный пиррол, например:

Реакции пиррола со слабыми электрофилами
Пиррол, обладающий высокой нуклеофильностью, легко вступает в реакции с такими слабыми электрофилами, с которыми бензол не реагирует даже в жестких условиях. Например, пиррол намного легче, чем даже фенолы, вступает в реакцию карбоксилирования (см. главу Фенолы) по Кольбе – достаточно нагревания с карбонатом аммония.

Пиррол, как и фенол, формилируется в условиях реакции Реймера-Тимана, когда в качестве активного реагента выступает дихлоркарбен (см. главу Алкилгалогениды. Реакции элиминирования). Однако данное взаимодействие осложняется параллельным процессом: происходит расширение цикла в результате внедрения дихлоркарбена в одну из π-связей пиррольного ядра, что приводит к 3-хлорпиридину. Объяснение этого состоит в том, что промежуточно образуется производное циклопропана, которое стабилизируется двумя альтернативными путями. Соотношение продуктов зависит от условий проведения реакции.

В слабокислой среде пиррол сравнительно устойчив, что позволяет ввести его, например, в реакцию азосочетания, которая еще раз подтверждает его высокую π-избыточность. Если пиррол вводить во взаимодействие с солью диазония в слабощелочной среде (реагирует пиррил-анион), то можно осуществить его превращение в 2,5-бис(фенилазо)пиррол.

Пиррол способен к конденсации с карбонильными соединениями по своим α-положениям, причем результат реакции зависит от природы альдегида или кетона. Если реакция с формальдегидом и алифатическими альдегидами в кислой среде дает в основном полимеры, то при конденсации с ацетоном основным продуктом оказывается метилированный порфириноген. Взаимное отталкивание в пространстве метильных групп способствует планаризации интермедиата – тримера, поэтому в ходе следующей стадии легче образуется циклический тетрамер, чем линейный.

При взаимодействии пирролов с ароматическими альдегидами по аналогичному механизму образуются порфириногены, которые, однако, самопроизвольно окисляются кислородом воздуха в ароматические мезо-тетраарилпорфирины.

В случае конденсации пиррола с пара-диметиламинобензальдегидом в слабокислой среде могут быть выделены первичные продукты конденсации – красно-фиолетовые соли арилиденпирроления (цветная реакция Эрлиха).

Для получения незамещенных порфириногена и порфирина пиррол предварительно превращают в свободное основание Манниха, а уже затем проводят конденсацию. Незамещенный порфириноген под действием мягких окислителей, например, при нагревании в хлороформе с хлоранилом, превращается в незамещенный порфирин – порфин.
