Стереоизомерия
Прохиральные центры. Энантиотопия и диастереотопия
В некоторых молекулах существуют одинаковые геминальные атомы или группы атомов, которые не совмещаются при повороте молекуле. Такие атомы (группы) не являются эквивалентными, а относятся друг к другу как предмет к зеркальному отражению.

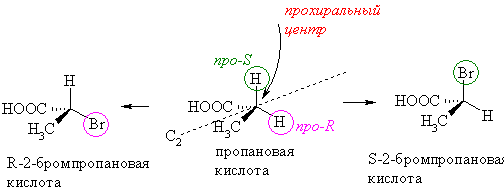
Например, в молекуле пропановой кислоты имеется поворотная ось симметрии С2, но атомы водорода в метиленовой группе неэквивалентны. При замещении на бром одного или другого образуются разные молекулы – энантиомеры 2-бромпропановой кислоты. Атом углерода, связанный с подобными группами называется прохиральным, одинаковые атомы или группы атомов, при замещении которых образуются энантиомерные молекулы называются энантиотопными (topos – подобие, др.словами – подобный энантиомерному).
Если энантиотопные атомы (группы) присутствуют в хиральной молекуле (уже имеющей элемент хиральности), то такие атомы (группы) называют диастереотопными. Таковыми являются, например, метиленовые атомы водорода в бутаноле-2. При замещении одного или другого из них образуются диастереомеры. Диастереотопные атомы (группы) в отличие от энантиотопных находятся в различном пространственном окружении и различаются физическими (например, дают разные сигналы в спектрах ЯМР) и химическими свойствами (с различной скоростью реагируют даже с ахиральными реагентами).
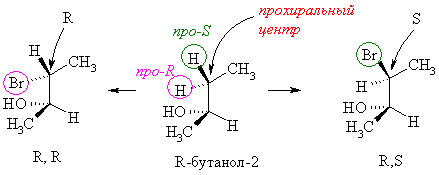
Энантиотопные и диастереотопные атомы, группы делят на про-R (pro-R) и про-S (pro-S). Если условно принять, что один из энанатиотопных (диастереотопных) заместителей старше другого, то заместитель будет про-R, если воображаемый хиральный центр будет иметь R-конфигурацию и про-S, если S -конфигурацию.
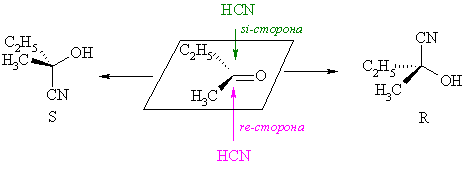
В плоских (тригональных) молекулах различают энантиотопные и диастереопопные поверхности. Так, в несимметричных карбонильных соединениях прохиральным центром является карбонильный атом углерода. В зависимости от атаки реагента – "сверху" или "снизу" молекулы образуются два энантиомера. Плоскости молекулы обозначают "re-" (если смотреть со стороны этой плоскость, то старшинство заместителей уменьшается по часовой стрелке) и "si-" (против часовой стрелки).
Энантиомерный состав нерацемического вещества характеризуют безразмерной мольной долей, которая называется энантиомерной чистотой или энантиомерным избытком (enantiomeric excess, ee).
eе = 100(хR – xS)/(хR + xS), где х – мольные доли энантиомеров.
Для нерацемической смеси с соотношением 80:20, ее = 60 %.
Величину оптической чистоты (optical purity, op) рассчитывают по формуле op = 100([α]/[α]max), где [α]max – удельное вращение энантиомерно чистого образца. Это понятие с конца 1980-х годов используется все реже, вытесняясь энантиомерным избытком. Действительно, ведь существуют энантиомерно чистые образцы веществ, которые не проявляют оптической активности.
Для определения ее используют следующие методы:
Хироптические методы – измерение удельного оптического вращения, расчет op. В идеале значения ее и ор должны совпадать, однако, это происходит далеко не всегда. Значение [α] зависит от множества факторов – температуры, растворителя, длины волны и пр., поэтому можно использовать [α] и [α]max измеренные в абсолютно идентичных условиях. Использование более современных физико-химических методов показало, что ранее рассчитанные с использованием хироптических методов значения ее зачастую неверны.
Спектроскопию ЯМР в хиральных растворителях (хиральные сольватирующие агенты). При регистрации спектров в нерацемических растворителях два энантиомера одного соединения дают неэквивалентные спектры ЯМР. Используя значения интегральной интенсивности, рассчитывают ее. Нет необходимости всегда использовать хиральный растворитель. Часто вместо него применяют хиральные сольватирующие агенты (ХСА) – реагенты, которые в некоторой степени участвуют в комплексообразовании с исследуемым веществом. Наиболее часто используемые ХСА:
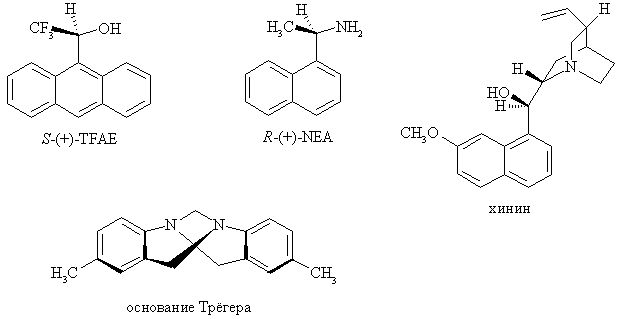
ЯМР диастереомеров, получаемых с помощью хиральных дериватизирующих агентов (ХДА). В этом методе проводят реакцию исследуемого образца с ХДА и измеряют ЯМР смеси. Некоторые ХДА содержат атомы фтора или фосфора, что позволяет использовать спектры ЯМР на ядрах 19F и 31P. Существенным ограничением является то, что ХДА должен быть энантиомерно чистым. ХДА для различных классов соединений:
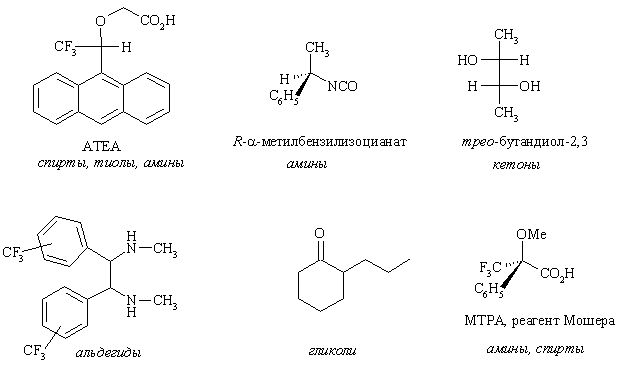
ЯМР с использованием хиральных сдвигающих реагентов (ХСР, ЛСР, шифт-реагентов) – трис-хелатных комплексов лантанидных металлов с кетонами. ХСР ассоциируется с полярными функциональными группами (амино-, амидо-, сложноэфирной, карбонильной, сульфокси- и др.) в молекуле, вызывая сдвиг в слабое поле сигналов близлежащих протонов. Например соединение европия Eu(hfc)3 и его ассоциация с карбонильными соединениями:
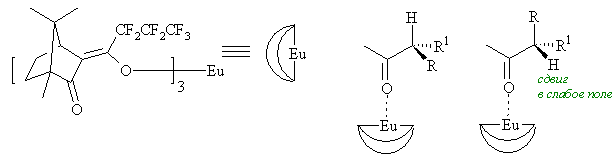
ХСР применяют для ядер Н, С, F. Различия в хим. сдвигах ядер Н в двух энантиомерах лежат в пределах 0,1-0,5 м.д. Степень энантиомерной чистоты ХСА не влияет на точность определения энантиомерного состава (хотя с уменьшением ее ХСА уменьшается разрешение энантиотопных сигналов). По сравнению с ХСА и ХДА ХСР обладают многими преимуществами: удобство метода (нет необходимости проводить химическую реакцию, как с ХДА, отсутствует необходимость количественного протекания реакции), более мягкие требования к энантиомерной чистоте реагента.
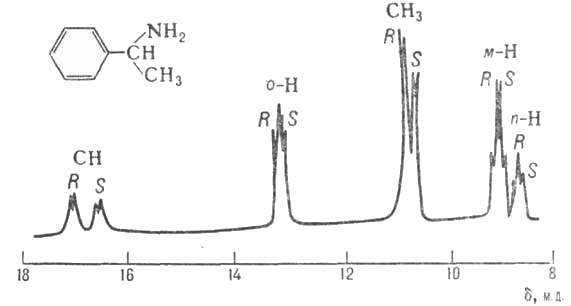
Спектр ПМР раствора смеси R- и S-изомеров
α-фенилэтиламина в СCl4 в
присутствии трис-(3-трет-бутилоксиметилен-(+)-камфорато)европия(III).
Хроматографические методы.
Газовая хроматография с ХДА. Проводят реакцию образца хирального соединения с ХДА, анализируют ГХ смеси диастереомеров. Основное требование к ХДА – 100 % ее. Применение метода ограничено летучими соединениями с умеренной термической стабильностью. Некоторые ХДА, используемые для определения энантиомерного состава методом ГХ:
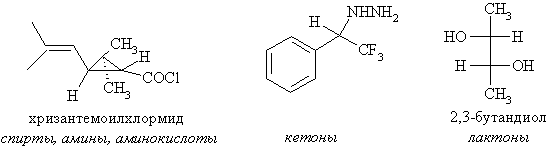
Высокоэффективная жидкостная хроматография с ХДА. Метод лишен основного недостатка ГХ, более универсален. Главные типы ХДА – ацилирующие агенты (используются для определения энантиомерного состава спиртов, аминов, аминокислот), амины (для карбоновых кислот), изоцианаты (для спиртов, аминов, лактамов). Некоторые ХДА для ВЭЖХ:
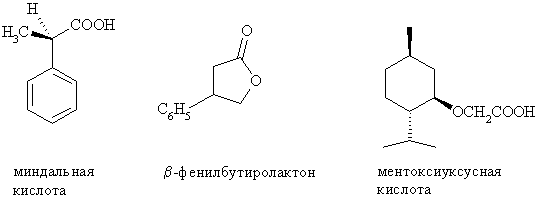
ВЭЖХ с использованием хиральных подвижных фаз вместе с ахиральными стационарными фазами. С помощью растворителей, содержащих добавки камфары, производных винной кислоты, алкалоиды, определяют ее различных хиральные соединений. Расщепление сигналов обусловлено образованием мигрирующих с разной скоростью диастереомерных димеров, образованных путем водородных связей или электростатических сил.
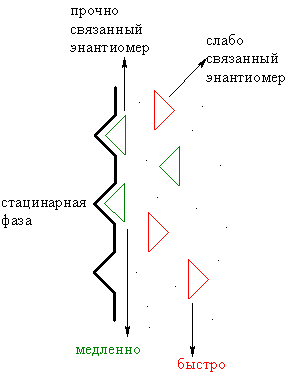
ВЭЖХ и ГХ на хиральных стационарных фазах. Два энантиомера реагируют с хиральной стационарной фазой с образованием переходных диастереомерных комплексов различной устойчивости. В качестве хиральных стационарных фаз используют углеводы (циклодекстрины), краун-эфиры, белки, фторированные спирты и др.
Правая и левая перчатки с одинаковой скоростью укладываются в прямоугольную коробку. А теперь попробуйте надеть эти перчатки на левую руку. Левая надевается быстро и хорошо, а правая – нет. В нашем случае перчатки – энантиомеры, коробка – ахиральный объект, может быть и ахиральный носитель, ахиральная молекула и т.п., рука – хиральный объект.