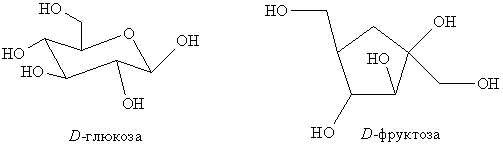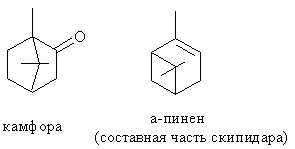
Стереоизомерия
Получение энантиомеров
Большинство реакций, в результате которых получаются энантиомеры, протекают не стереоселективно и в итоге с равной вероятностью образуются оба стереоизомера (т.е. образуется рацемат). Один из способов получения чистых энантиомеров – разделение (расщепление) рацематов.
Расщепление рацематов – разделение рацематов на два образующих его компонента. Способы расщепления:
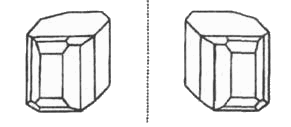
Сортировка кристаллов. В том случае, когда рацемат представляет собой конгломерат, то при кристаллизации вещество претерпевает спонтанное (самопроизвольное) расщепление. Это значит, что в процессе кристаллизации образуются два вида энантиоморфных кристаллов, каждый из которых состоит исключительно из молекул одного энантиомера. Ручная разборка кристаллов называется сортировкой. Этим способом впервые Пастером был разделен рацемический тартрат натрия-аммония.

Энантиоморфные кристаллы
тартрата натрия-аммония
Конгломератами являются только 5-10 % всех твердых хиральных соединений. Однако если само вещество и не дает конгломерата, то его можно превратить в простое производное, которое будет кристаллизоваться в виде конгломерата. Например, аминокислоты в большинстве случаев дают истинные рацематы, в то время как их бензолсульфонатные производные (в частности бензолсульфонаты аланина, лейцина, триптофана и др.) являются конгломератами. В целом частота образования конгломератов возрастает в том случае, если производное является солью, а не ковалентным соединением. Так, многие хиральные амины разделяют сортировкой кристаллов их солей.
В некоторых случаях образованию конгломерата способствует внесение затравки энантиомерно чистых кристаллов. При этом, если вносят кристаллы только одного энантиомера, то он преимущественно и кристаллизуется из раствора, тогда как второй остается в маточном растворе. Такой процесс называют избирательной кристаллизацией.
Большинство описанных расщеплений рацематов было выполнено через превращение рацемата в смесь диастереомеров. Образующиеся диастереомеры разделяют либо кристаллизацией, либо хроматографическими методами и проводят обратную реакцию превращения диастеремеров в исходные энантиомеры:
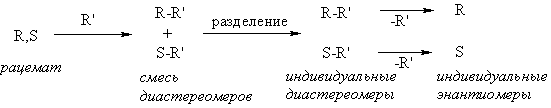
Расщепляющие реагенты должны обладать следующими характеристиками: доступность, в том числе доступность реагента с высокой энантиомерной чистотой; легкость как реакции с субстратом, так и регенерации; устойчивость, в том числе при хранении. Часто с этой целью используют природные хиральные соединения – например, бруцин, стрихнин, хинин, ментол, некоторые аминокислоты в качестве расщепляющих реагентов для кислот; винную, яблочную, миндальную кислоты – для оснований; глюкозу – для спиртов. Доказано, что для успешного разделения желательно чтобы между разделяемым субстратом и расщепляющим реагентом возникали множественные взаимодействия – т.е. желательно, чтобы расщепляющий реагент кроме основной функциональной группы имел и дополнительные функции и (или) ароматические кольца.
Соединения, лишенные обычных функциональных групп (хиральные алкены, арены, сульфоксиды, фосфины) разделяют путем образования диастереомерных комплексов. Например,
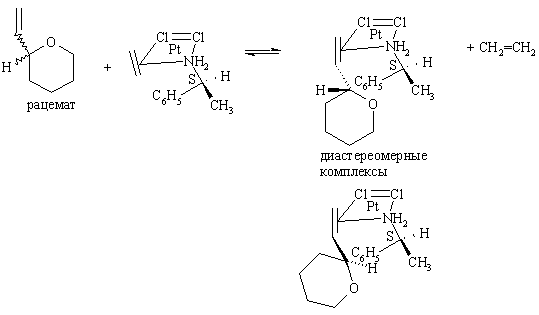
Кинетическое расщепление заключается в проведении реакции рацемата с хиральным (в некоторых случаях ахиральным) соединением. При этом один из энантиомеров реагирует быстрее, а второй – медленнее и некоторая его часть остается не прореагировавшей.
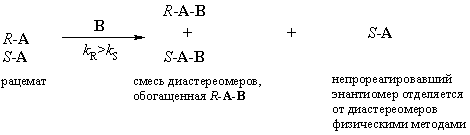
Например:
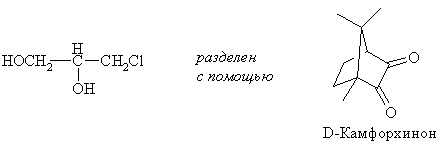
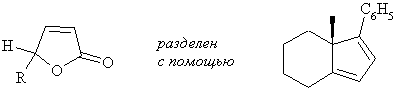
Наиболее широко применяют катализируемое ферментами кинетическое расщепление (ферментативное расщепление). Примеры: микробное разделение кислоты Мошера (выделяют R-энантиомер, ее 100 %); амиды аминокислот разделяют на энантиомеры в процессе гидролиза, катализируемого гидролазами (ацилазами); из двух энантиомеров 2-бромпропионовой кислоты с 1-бутанолом в присутствии липазы дрожжей реагирует только R-форма, S- остается без изменений (ее 99,6 %).
Все большее значение приобретают препаративные хроматографические методы разделения рацематов на нерацемических носителях. В качестве таких носителей используют циклодекстрины (макроциклические олигомеры глюкозы, из 6 и более глюкопиранозных остатков), свзанные с силикагелем; микрокристаллические простые и сложные эфиры и карбаматы целлюлозы (ChiralcelTM); хиральный изотактический поли(трифенилметилметакрилат) (PTrMA) – молекулы этого вещества обладают спиральностью. На PTrMA препаративно разделяют гексагелицен.
Энантиоселективный синтез
Стереоселективный (асимметрический) синтез – синтез, в ходе которого один из двух возможных стереоизомеров образуется в большем количестве, чем второй. Если исходные соединения и (или) продукты реакции могут существовать в двух или нескольких стереоизомерных формах, часто наблюдается преимущественное образование одного из возможных продуктов. Такое предпочтение одного пути реакции называется стереоселективностью. Она определяется как отношение разности количеств образующихся изомеров А и Б к их сумме (А – Б)/(А + Б). Протекание реакции исключительно по одному пространственному пути из нескольких возможных называют стереоспецифичностью, т. е. стереоспецифичной является полностью стереоселективная реакция.
Один из наиболее распространенных путей энантиоселективного синтеза – реакции нуклеофильного присоединения по карбонильной группе.
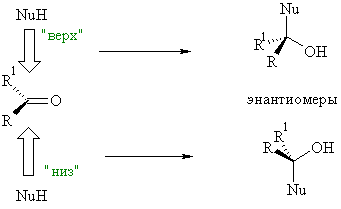
В обычных условиях нуклеофильное присоединение к альдегидам и несимметричным кетонам всегда приводит к рацемату. Чтобы подобная реакция стала энантиоселективной, используют хиральные реагенты, хиральные катализаторы или проводят реакцию в хиральной среде.
Восстановление с помощью хиральных реагентов. Асимметрический синтез оптически активных спиртов часто осуществляют восстановлением карбонильных соединений с помощью хиральных комплексов, образующихся при взаимодействии LiAlH4 или NaBH4 с оптически активными диаминами, аминоспиртами, диолами, углеводами.
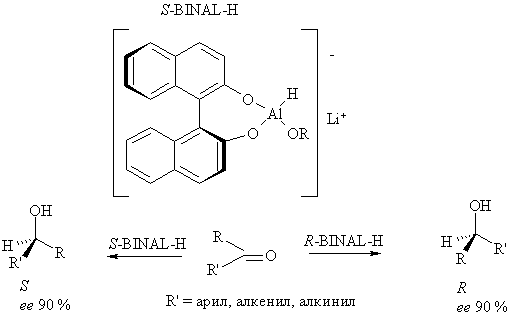
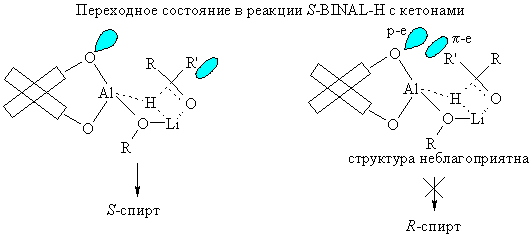
Высокие оптические выходы достигаются при использовании В-3-пинанил-9-борабицикло[3.3.1]нонана (пинанил-BBN, Alpine-Borane):
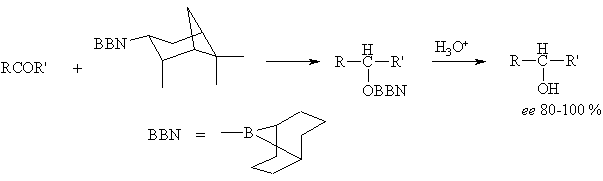
Присоединение металлорганических соединений. Вспомогательный хиральный конформационно жесткий комплекс, полученный из пролина, реагирует с карбонильными соединениями с образованием оптически активных спиртов.
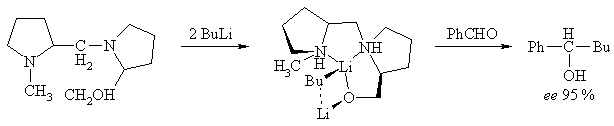
Энантиомерная чистота спиртов, полученных реакцией (3,3-диметилаллил)ди(пинанил-3-)борана с альдегидами достигает 96 %.
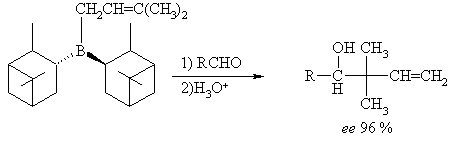
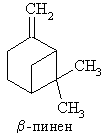
Несмотря на то, что энантиомеры хиральных органических соединений имеют различную растворимость в хиральных растворителях, использование последних в стереоселективных реакциях в большинстве случаев дает невысокие выходы ее (до 30 %). В качестве таких растворителей использовали эфиры винной кислоты, b-пинен, (+)-2,3-диметоксибутан.
Асимметрический катализ. Важное место в асимметрическом синтезе занимает асимметрический катализ, при котором асимметризующим агентом является катализатор.
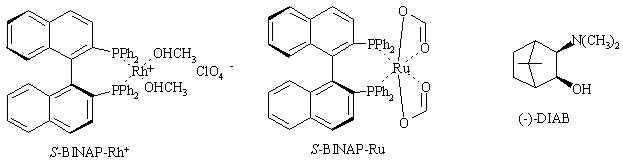
Гомогенный катализ с использованием хиральных катализаторов (родиево-фосфиновых, рутений-фосфиновых, металлических комплексов на основе борнана) – наиболее быстро развивающаяся область асимметрического катализа.
Например, родиевые и рутениевые комплексы на основе 1,1'-бинафтила (BINAP-Rh, BINAP-Ru) используют как катализаторы при энантиоселективном восстановлении кетонов. Борнановые комплексообразователи (DIAB) – для реакций кетонов с металлорганическими соединениями.
Абсолютный асимметрический синтез осуществляется в отсутствии асимметрических реагентов и катализаторов, при этом асимметризующее действие оказывает тот или иной физический фактор. Например, в асимметрических синтезах, в которых носителями для катализатора (металлы, щелочи) служат энантиоморфные кристаллы (оптически активного кварца), роль асимметризующего агента выполняет кристаллическая решетка носителя. Этим способом осуществлены (хотя и с ничтожными оптическими выходами) гидрирование рацемического пинена и α-фенилкоричной кислоты, цианэтилирование 2-метилциклогексанона. Механизм асимметризующего действия связан с неодинаковой адсорбируемостью энантиомеров на оптически активном кварце.
Синтезы на основе природных веществ. Природа предоставляет большое разнообразие асимметрических соединений в оптически чистой форме (сахара, стероиды, алкалоиды, аминокислоты, терпены и др.). Модификацией природных соединений получают различные оптически чистые вещества, используемые в медицине, фармакологии, сельском хозяйстве, в асимметрическом синтезе в качестве дополнительных хиральных компонент и др. Некоторые природные энантиомерно чистые вещества: